Tomar una ranitidina es común para combatir el dolor de estómago, sin embargo, consumirla puede traer más consecuencias de las que imaginamos:
Recientemente se dio a conocer que 42 empresas farmacéuticas mexicanas compraron materia prima contaminada con NDMA, un agente cancerígeno.
La ranitidina contaminada fue adquirida en India y China, países donde su adquisición es barata y no cuentan con procesos completos de purificación.
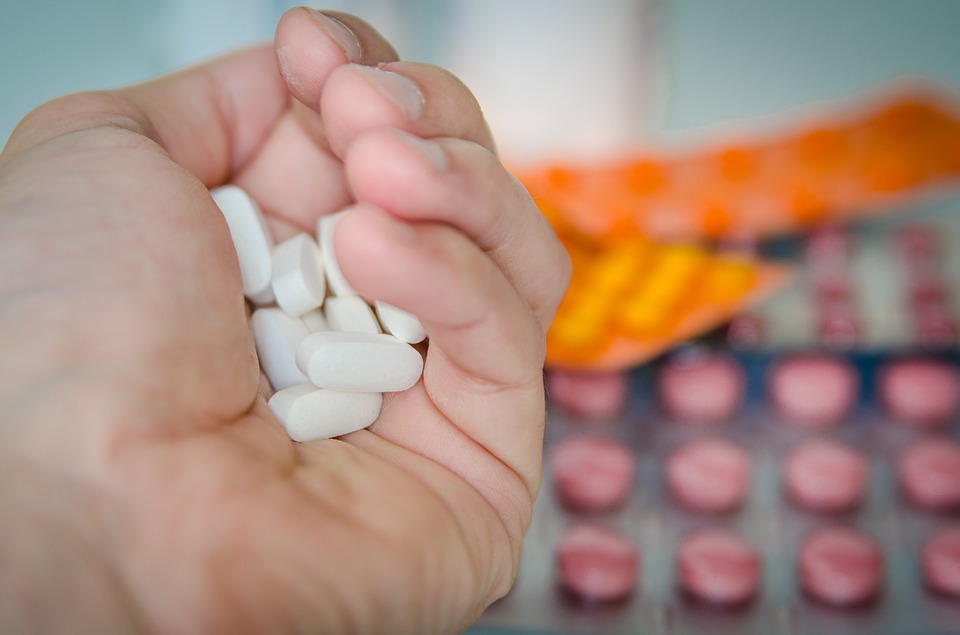
De acuerdo con Gilberto Castañeda de Farmacología del Centro de Investigación y de Estudios Avanzados (Cinvestav) del Instituto Politécnico Nacional, la contaminación por el agente NDMA en productos con ranitidina fue una alerta a nivel mundial y que en México afectó a 42 empresas que producen o comercializan el medicamento genérico, con el fin de ahorrar costos.
“Hay empresas que están comprando materias que no deberían comprar. En el caso de la ranitidina, nos están indicando que varias compañías, por cuestiones de ahorro o disminución de costos, compran materias primas y no hacen pruebas de calidad”.
Castañeda afirma que para la elaboración de ranitidina ,el principio activo que ayuda a tratar úlceras y acidez estomacal, las compañías farmacéuticas compran materia prima en el mercado internacional con compuestos casi siempre derivados del petróleo.
Dichos compuestos se sintetizan y se van modificando hasta obtener el activo final. en el proceso químico se van quedando contaminantes como la N-nitrosodimetilamina (NDMA), que se tienen que eliminar con un proceso de purificación.
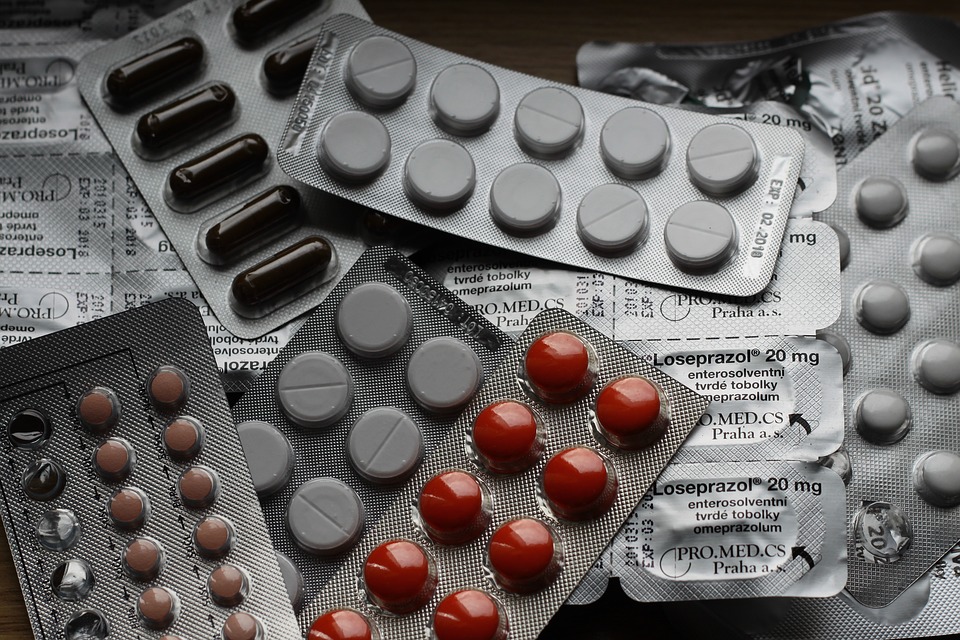
Responsabilidad de las farmacéuticas
La postura que están tomando las farmacéuticas es la correcta debido a que ellas están evitando que el consumidor adquiera este tipo de medicamentos y dañe su salud o la de sus familiares.
De esta manera están cuidando al consumidor y están ejerciendo su responsabilidad social para no afectar a n adie.
Y es que según la Administración de Alimentos y Drogas del gobierno de Estados Unidos (FDA, por sus siglas en inglés), dice que los niveles máximos que debe contener cada dosis de ranitidina es de 0,32 partes por millón para que no sea dañino en personas que utilicen el medicamento diario.
Gilberto Castañeda dice que “con el propósito de ahorrar y disminuir costos, muchas compañías compran la materia prima a proveedores de países como India y China y para que salga más barato, hacen procesos de purificación que no están completos, entonces la concentración del NDMA queda en límites superiores a lo permitido”.
Esto no quiere decir que el medicamento se compre contaminado con el fin de ahorrar, sino que las empresas mexicanas no realizan su propio proceso para verificar la calidad del compuesto que después venden en el país.
Malos procesos de calidad
Las farmacéuticas están obligadas a tener especificaciones técnicas para todo lo que compran, “por eso cuando llega cualquier insumo no se debe usar así nada más, sino que se tiene que tener un control de calidad. Si se compra ranitidina procedente de china, antes de usarlo se tiene que tomar una muestra y ver que cumpla con las especificaciones, eso es lo que no están haciendo porque tiene un costo. Ahí sí se ahorran un dinero, pero ponen en peligro a la gente”.
Para adquirir el medicamento no se necesita receta y normalmente es usada para prevenir y aliviar la acidez estomacal asociada con la indigestión ácida. Por ello, las farmacéuticas decidieron no vender más este tipo de producto.
Hace unas semanas, la Comisión Federal para la Protección Contra Riesgos Sanitarios (Cofepris) pidió dejar de consumir ranitidina tras confirmar el ingrediente y dijo que es necesario evitar la compra este medicamento:
- Al personal médico, no prescribir medicamentos que contengan Ranitidina, considerar otras alternativas terapéuticas, además de reportar cualquier reacción adversa relacionada con este tipo de medicamentos, a esta COFEPRIS a través de e-reporting, disponible en la sección de Farmacovigilancia o en el correo electrónico [email protected]
- A farmacias y distribuidores, suspender la comercialización de los
medicamentos que en su formulación contengan Ranitidina, en tanto se toman las medidas que garanticen la seguridad del producto. - A los titulares de los registros sanitarios de los medicamentos que contienen en su formulación Ranitidina, suspender la fabricación, distribución y venta de estos productos, en tanto se toman las medidas que garanticen la seguridad del producto.
En países como Estados Unidos, Canadá, Francia, España, Australia, Austria, Bélgica, Alemania y Suecia, se decidió retirar del mercado medicamentos con este fármaco. Sin embargo, en México, lo siguen vendiendo, sobre todo en farmacias pequeñas.
#Comunicado ? La @Cofepris informa sobre los productos que contienen en su formulación el principio activo denominado #Ranitidina ? https://t.co/pTqC6bjtVI @SSalud_mx pic.twitter.com/XovvYejLgU
— COFEPRIS (@COFEPRIS) October 6, 2019












